Kiaušidžių vėžys (KV) yra dažniausia moterų mirtingumo nuo onkoginekologinių ligų priežastis. KV dažniausiai nustatomas III–IV stadijos, nes ligos klinikinė eiga nėra specifinė, nėra efektyvių ankstyvosios diagnostikos metodų [1]. 2018 metais pasaulyje nuo šios ligos mirė maždaug 184 tūkst. moterų [2]. Didelio piktybiškumo serozinė kiaušidžių karcinoma (angl. high-grade serous ovarian carcinoma) pasižymi didžiausiu mirtingumu. Šis vėžio tipas sudaro 60–80 proc. kiaušidžių vėžio atvejų. Daugiau nei 88 proc. didelio piktybiškumo serozinė kiaušidžių karcinoma diagnozuojama III–IV stadijos, o penkerių metų išgyvenamumas sergant šio tipo kiaušidžių vėžiu siekia 9 proc. [1]. Tradiciniai KV diagnostikos metodai yra: transvaginalinė echoskopija (TVE), kraujo serumo testai: karbohidratų antigeno 125 (CA125) ir žmogaus epidermio baltymo 4 (HE4) ± ROMA indeksas (angl. Risk of Ovarian Malignancy Algorithm). Atlikta nemažai klinikinių tyrimų, kuriuose siekta nustatyti KV patikros metodų efektyvumą, pavyzdžiui, PLCO, UKCTOCS, ROCA, GOGo199. Juose gauti rezultatai labai panašūs – tokia patikra (CA125 ir TVE) nesumažina mirtingumo nuo KV. Taikant šiuos tyrimo metodus ankstyvajai KV diagnostikai, padidėja nereikalingų chirurginių intervencijų skaičius: remiantis UKCTOCS tyrimu, 2 iš 3 operacijų nebuvo nustatyta KV, o PLCO tyrimo duomenys parodė, jog vienam vėžio atvejui nustatyti reikia atlikti iki 20 biopsijų. Vėžio žymuo CA125 pasižymi nedideliu jautrumu. CA125 padidėja sergant ne tik KV, bet ir gerybine patologija, gimdos kaklelio, storosios žarnos, krūties ir plaučių vėžiu [3, 4].
KV patogenezė
Norint sukurti ankstyvosios KV diagnostinius metodus, svarbu suprasti ligos patogenezę. Dauguma KV atvejų susiformuoja ne iš kiaušidžių audinio, o kiaušintakių epiteliui implantuojantis kiaušidėse, kurios pasižymi navikams palankia mikroaplinka. Įvykus implantacijai, kiaušidės yra aktyvinamos, ima sekretuoti steroidinius hormonus (estrogeną, progesteroną ir androgenus), kurie stimuliuoja epitelio augimą. Kiaušintakių epitelis gali sudaryti cistas, kuriose vyksta piktybinė transformacija. Anksčiau buvo manoma, kad didelio piktybiškumo serozinė kiaušidžių karcinoma išsivysto dėl nepertraukiamos ovuliacijos – pasikartojančio kiaušidžių audinio sužalojimo per kiekvieną ovuliacijos ciklą. Pasikartojantis sužalojimas sukelia padidėjusį uždegimą ir hormonų lygio pokyčius, sukeliančius DNR pažeidimus ir oksidacinį stresą [4]. KV navikų molekulinė analizė parodė, kad didelio patogeniškumo KV atvejai yra kilę iš kiaušintakių karcinomų (angl. Serous tubal intraepithelial carcinoma – STIC). SEE–FIM (angl. Sectioning and Extensively Examining the FIMbriated end) protokolas buvo sukurtas siekiant sistemingai įvertinti BRCA1/2 patologijų nešiotojų kiaušintakius. Jis leido dažniau nustatyti ankstyvas serozines karcinomas kiaušintakio distaliniame gale, kurių dauguma buvo lokalizuotos kiaušintakių fimbrijose STIC. 92 proc. STIC atvejų yra nustatomos TP53 geno patologijos, sutampančios su patologijomis, nustatytomis sergant KV. Taigi STIC yra KV pirmtakai, o ne metastazės. Apie 15 proc. pacienčių, kurioms nustatytos BRCA1/2 patologijos, yra atliekama abipusė salpingooforektomija, siekiant sumažinti riziką susirgti KV [5].
KV tipai
Viena pagrindinių priežasčių, kodėl KV išlieka daugiausiai mirčių sukeliančia ginekologine liga, yra šios ligos heterogeniškumas. Pagal XXI amžiaus KV patogenezės teoriją [5], KV galima suskirstyti į 2 grupes:
- vadinamąjį kiaušidžių kilmės KV (lytinės drūžės navikai, germinacinių ląstelių navikai);
- vadinamąjį ne kiaušidžių kilmės (angl. extraovarian origin) KV, kuriam priklauso I ir II tipo epiteliniai navikai.
Abiejų grupių KV vystosi skirtingais molekuliniais patogenezės mechanizmais. Ši teorija leidžia daryti prielaidą, kad tikrieji kiaušidžių navikai (kiaušidžių kilmės) yra tik lytinės drūžės-stromos ir germinogeniniai navikai, analogiški sėklidžių navikams, o ne kiaušidžių kilmės navikai vystosi audiniuose, esančiuose už kiaušidės ribų, ir tik vėliau įtraukia kiaušides, arba iš šių audinių implantų kiaušidės kapsulėje [5]. Priklausomai nuo patogenezės, skiriami 2 ne kiaušidžių kilmės vėžio tipai (1 pav.).
1 pav. KV karcinomų tipai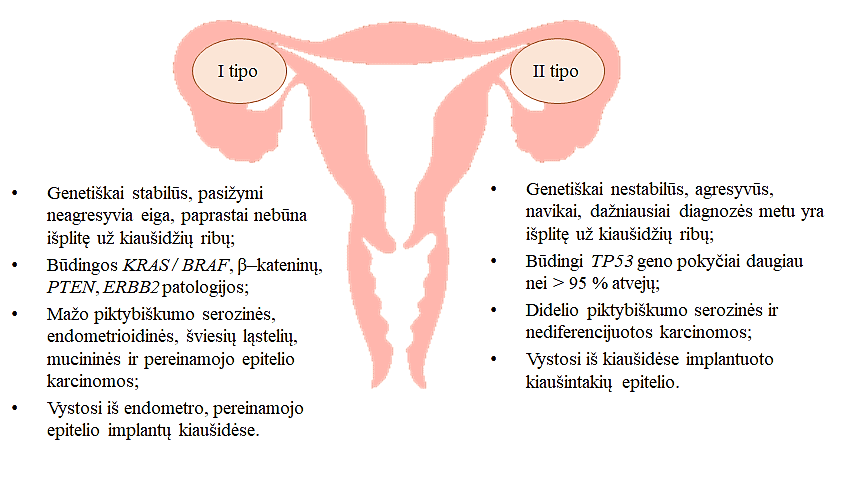
- I tipo navikai vystosi iš gimdos gleivinės arba pereinamojo epitelio ląstelių implantų kiaušidėse. Pradžioje susidaro gerybiniai dariniai (mucininė cistadenoma, endometrioma, serozinė cistadenoma ar Brenerio navikas), ilgainiui vystosi ribinio piktybiškumo navikai, o vėliau endometriodinė, šviesiųjų ląstelių, mucininė, mažo piktybiškumo serozinė karcinoma. Šio tipo KV paprastai yra nustatomas I stadijos, prieš išplintant už kiaušidžių ribų, o navikai yra genetiškai stabilūs, priklausomi nuo estrogenų, ir pasižymi lėta vystymosi eiga, siejama su KRAS, BRAF, PTEN, PIK3CA, CTNNBI, ARID1A ir PIK2R1 genų patologijomis, kurios sutrikdo ląstelių signalinius kelius ir lemia vėžio vystymąsi [6, 7]. Maždaug 20 proc. I tipo KV atvejų nustatomos PTEN ar PIK3CA patologijos, kurios aktyvina PI3K/PTEN signalinį kelią: PTEN inaktyvinimas daro įtaką fosfatidilinozitolio(3,4,5)-trifosfato (PIP3) ir baltymų kinazės B (PKB ir AKT) raiškai, taip sumažinant baltymų fosfatazės aktyvumą ir skatinant ląstelės ciklo progresiją. 40 proc. I tipo KV atvejų pasižymi Wnt / β-kateninų signalinio kelio aktyvinimu, dažniausiai CTNNB1 geno, koduojančio β-kateniną, patologijomis [6]. Maždaug 65 proc. atvejų nustatytos KRAS ir BRAF patologijos, kurios dalyvauja mitogenų aktyvinamos baltymų kinazės (MAPK) signaliniame kelyje [8]. Šių signalinių kelių aktyvinimas yra svarbi vėžinių ląstelių proliferacijai ir išgyvenamumui.
- Skirtingai nei I tipo navikai, II tipo KV sudaro iki 80 proc. kiaušidžių piktybinių navikų. Šio tipo KV startinis patogenezės momentas – pakitimai kiaušintakių fimbrijų epitelyje, vadinami STIL (angl. serous tubal intraepithealial lesion) – normaliai atrodantis kiaušintakio epitelis, kuriam būdinga padidėjusi p53 raiška, vėliau pereina į STIC, kuri ilgainiui vystosi į invazyvinę didelio piktybiškumo serozinę karcinomą. Navikinės ląstelės implantuojasi kiaušidžių, pilvaplėvės audiniuose. Tai genetiškai nestabilūs, agresyvūs navikai, diagnozuojami jau išplitę už kiaušidžių ribų – didelio piktybiškumo serozinė karcinoma, nediferencijuota karcinoma. Charakterizuojamas somatinėmis TP53 patologijomis, kurios nustatomos 96 proc. II tipo navikų, ir retesnėmis NF1, BRCA1/2, RB1, PIK3CA, PP2R1A ir CDK12 mutacijomis, tetraploidija ir homologinės rekombinacijos defektais, susijusiais su dažnu (apie 22 proc. atvejų) BRCA patologijų dažniu [6, 7, 8]. Daugiau nei 75 proc. atvejų nustatomas jau pažengęs (II–IV stadijos) II tipo KV, o tai lemia nedidelį išgyvenamumą [6].
Įgyvendinat Vėžio genomo atlaso projektą (angl. The Cancer Genome Atlas Research Network – TCGA), buvo atlikta išsami KV genomo analizė. KV atvejai pagal genų patologijas suklasifikuoti į 4 grupes:
1) dažnų POLE patologijų;
2) hipermutacijų / nestabilių mikrosatelitų;
3) mažo kopijų skaičiaus / stabilių mikrosatelitų;
4) didelio kopijų skaičiaus (panašių į serozinį tipą) mutacijų (2 pav.) [8].
2 pav. TCGA (angl. The Cancer Genome Atlas) klasifikacijos sistema klinikinei KV diagnozei [9]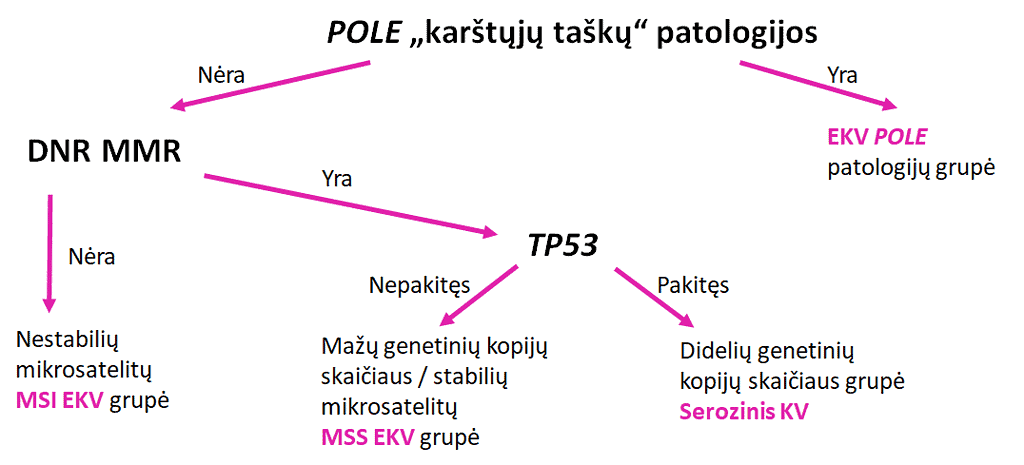
Pirmoji grupė pasižymi itin dideliu patologijų dažniu (232×10-6 mutacijų megabazei, Mb), C→A transversijų skaičiumi, daugiausiai DNR polimerazės epsilon (POLE), dalyvaujančios DNR replikacijoje ir reparacijoje, kataliziniame domene. Dažnos patologijos nustatytos PTEN, PIK3R1, PIK3CA, FBXW7 ir KRAS genuose, tačiau šioje grupėje retai pasitaiko mikrosatelitų (trumpų 1–6 nukleotidų ilgio pasikartojančių DNR sekų) skaičiaus pokyčių. Ši grupė pasižymi ilgiausiu išgyvenamumu iš visų 4 KV grupių [9]. Nestabilių mikrosatelitų (angl. microsatellite unstable – MSI) grupė, palyginti su stabilių mikrosatelitų (angl. microsatellite stable – MSS) grupe, pasižymi maždaug 10 kartų didesniu mutacijų dažniu (18×10-6 vs. 2,9×10-6 patologijų per Mb). MSI kyla dėl DNR neteisingai suporuotų nukleotidų reparacijos sistemos defektų, dėl kurių padidėja tandeminių pasikartojimų skaičius [10]. MSI grupė pasižymi mutacijomis RPL22, FBXW7, CTNNB1, PPP2R1A ir TP53 genuose bei neteisingai suporuotų nukleotidų reparacijos geno MLH1 promotoriaus metilinimu, dėl kurio sumažėja geno raiška. Ši grupė apima serozinius ir didelio piktybiškumo endometriodinius navikus. MSS grupėje CTNNB1 yra vienintelis genas, pasižymintis didesniu patologijų dažniu nei MSI grupėje. Dėl šio geno pokyčių gali sutrikti Wnt kelio signalinė grandinė. 4 grupė, sudaryta daugiausiai iš serozinių navikų, pasižymi dideliu TP53 patologijų dažniu (90 proc.), taip pat MYC, ERBB2, CCNE1, FGFR2 ir SOC17 onkogenų sekų amplifikacija, tačiau mažu MSI dažniu (6 proc.) [7].
Histologinė klasifikacija yra plačiausiai paplitęs KV klasifikacijos būdas, bet TCGA parodė, kad maždaug penktadalis KV atvejų, klasifikuotų kaip 3 diferenciacijos laipsnio endometriodiniai navikai, molekuliniu lygmeniu labiau primena serozinius (II tipo) navikus. Šie navikai pasižymi TP53 patologijomis, taip pat dažnomis FBXW7 ir PPP2R1A patologijomis, retai pasireiškiančiomis endometriodiniuose navikuose, taip pat onkogenų MYC, CCNE1, FGFR3, SOX17 ir ERBB2 amplifikacijomis. ERBB2 amplifikacija nustatoma 25 proc. serozinių ir į serozinius panašių navikų biopsijose, kuri yra svarbi parenkant gydymo kursą, nes tokie navikai gali būti gydomi ERBB2 inhibitoriais [7].
TP53 mutacijos – pagrindinė II tipo KV priežastis
TP53 genas, kurio patologijos nustatomos beveik visais II tipo KV atvejais, yra daugiausiai patologijų turintis navikų supresorius. Šio geno pokyčiai nustatomi daugiau kaip pusėje visų žmonių navikų, todėl TP53 yra vienas geriausiai ištirtų genų pasaulyje [11]. TP53 koduoja transkripcijos veiksnį p53, valdantį atsaką į DNR pažaidas. Esant normaliai ląstelės būsenai, E3 ubikvitino ligazė MDM2 palaiko nedidelį p53 kiekį ląstelėje. P53 yra aktyvinamas ląstelinio streso, kurį sukelia DNR pažaidos, hipoksija, onkogenų aktyvinimas ir ribosominio streso metu, p53 yra fosforilinamas ir šio baltymo nebeveikia ubikvitino ligazė. Kaip atsaką į DNR pažaidas p53 aktyvina genų raišką, dalyvaujančių DNR pažaidų atsake (pvz., genų DDB2 ir XPC), ląstelės ciklo sustabdyme (nuo ciklinų priklausomos kinazės inhibitorio 1 (CDKN1A), koduojančio p21), apoptozėje (PUMA ir BAX), ląstelės metabolizme (TP53 indukuotos glikolizės ir apoptozės reguliatorio (TIGAR)) ir savo paties reguliacinėse grandinėse (MDM2 ir p53 indukuotos fosfatazės 1) [12].
Dažniausiai pasitaikančios TP53 geno patologijos įvyksta 5–8 egzonuose ir yra aminorūgštį pakeičiantys pokyčiai, dažniausiai keičiantys baltymo p53 domeną, kuriuo šis jungiasi prie DNR. Tokios patologijos sukelia p53 baltymo raiškos stabilizaciją, todėl sutrinka normalus ląstelės ciklas [11]. Maždaug 20 proc. KV atvejų įvyksta onkomorfinės TP53 mutacijos, pakeičiančios p53 funkciją ir taip prisidedančios prie vėžio progresijos ir nejautrumo chemoterapijai. Nustatyta, kad pacientai, kuriems nustatytos onkomorfinės mutacijos, turi prastesnius išgyvenamumo ir dažnesnius atsparumo platinos chemoterapijai rodiklius [13].
87 proc. KV atvejų turi patologijas genuose, susijusiuose su TP53 signaliniu keliu, tokiuose kaip FOXM1 ir jo valdomuose genuose AURKB, CCNB1, BIRC5, CDC25 bei PLK1, kurių raiška yra susijusi su vėžinių ląstelių proliferacija ir DNR pažaidų atsaku. Normaliose ląstelėse, esant DNR pažaidoms, p53 inaktyvina FOXM1, tačiau patologijos padidina FOXM1 raišką ir sutrikdo normalius signalinius kelius bei pradeda ląstelių transformaciją į vėžines ląsteles. Dėl šių priežasčių TP53 patologijos yra laikomos viena pagrindinių II tipo KV priežasčių [14].
KV skystosios biopsijos tyrimai
Norint pritaikyti molekulinę KV klasifikaciją, būtina rasti paprastų ir neinvazinių būdų nustatyti vėžio tipą. Pastaruoju metu KV diagnostikoje siekiama pritaikyti skystosios biopsijos tyrimus, kai iš kraujo, šlapimo, gimdos nuoplovų ar kitų kūno skysčių išskirtose cirkuliuojančiose navikų ląstelėse, egzosomose ar nukleorūgštyse būtų nustatomi biožymenys, padedantys nustatyti ligą ir jos tipą.
Cirkuliuojanti DNR (angl. cell-free DNA – cfDNR) yra vienas perspektyviausių vėžio biožymenų, kuris jau yra efektyviai pritaikytas nesmulkialąstelinio plaučių vėžio tyrimuose. CfDNR dažniausiai yra trumpi (70–200 bp) dvigrandžiai DNR fragmentai, kurie apoptozės ar nekrozės metu atpalaiduojami iš ląstelių. CfDNR kiekis vėžiu sergančių pacientų kūno skysčiuose yra didesnis už sveikų asmenų, cfDNR nustatytos patologijos atitinka navikinės DNR patologijos [15]. Nors cfDNR kiekis skystosios biopsijos mėginiuose dažniausiai yra labai nedidelis (gali sudaryti mažiau nei 0,01 proc. mėginio), cfDNR galima nustatyti jautriais ir specifiškais kiekybinio PGR, naujos kartos sekoskaitos ar kitais molekuliniais metodais [16].
Swisher ir bendraautorių atliktame tyrime 93 proc. (28/30) moterų, sergančių KV, nustatyta TP53 patologijų cfDNR, išskirtoje iš pilvaplėvės nuoplovų [17]. Erickson ir bendraautorių bandomajame tyrime 3 iš 5 II tipo KV pacienčių DNR mėginių, gautų iš makšties tamponų, detektavo TP53 somatines patologijas (jautrumas 60 proc.) [18]. DNR metilinimo tyrimu nustatytas padidėjęs 9 genų metilinimas 38 KV skystosios biopsijos mėginiuose, gautuose iš tamponų [19]. Viename naujausių tyrimų Nair su bendraautoriais, sekvenuodami gimdos nuoplovų mėginius, nustatė su KV siejamas patalogijas 7 pacienčių, sergančių I stadijos KV, mėginiuose. Dar 51 pacientei, kuriai histologiniais tyrimais nenustatytas KV, diagnozuota su vėžiu susijusi patologija [20].
2018 metais KV diagnostikai buvo pasiūlytas PapSEEK testas, kai naujos kartos sekoskaitos metodais tiriama 18 genų sritys ir aneuploidijos. 81 proc. moterų, sergančių epiteliniu KV, nustatytos patologijos gimdos kaklelio tepinėliuose (kūno skysčiuose, gautuose Papanicolaou (PAP) tyrimo, paprastai taikomo gimdos kaklelio vėžio diagnostikoje, metu). Dar didesnis kiekis patologijų (93 proc.) nustatytas tepinėliuose, gautuose iš gimdos (Tao tepinėlis); šie tyrimai pasižymėjo didesniu 99 proc. specifiškumu. Tepinėliuose dažniausiai pasitaikančios patologijos: PTEN (63 proc.), TP53 (42 proc.), PIK3CA (36 proc.), PIK3R1 (20 proc.), KRAS (17 proc.), CTNNB1 (15 proc.), FGFR2 (15 proc.), RNF43 (11 proc.), PPP2R1A (7 proc.), POLE (7 proc.) ir FBXW7 (6 proc.). Tame pačiame tyrime daliai moterų (n=83) buvo tirtos mutacijos ne tik PAP tepinėlyje, bet ir kraujo plazmoje, tačiau tik 17 mėginių sutapo nustatytos patologijos [19]. Nors PapSEEK tyrimas pasižymi itin dideliu specifiškumu, o tyrimas gimdos nuoplovose pasižymi dideliu jautrumu, reikia atlikti daugiau tyrimų, siekiant pritaikyti skystosios biopsijos metodus KV diagnostikai ir gydymui.
Apibendrinimas
Genetinių patologijų tyrimai skystosios biopsijos mėginiuose galėtų padėti anksčiau ir lengviau nustatyti KV, tačiau būtina identifikuoti informatyviausius KV genetinius žymenis ir sukurti klinikinei diagnostikai tinkamus tyrimų metodus.
Gyd. Diana Žilovič1, 2, Ieva Vaicekauskaitė1, 2, gyd. Rūta Čiurlienė1, dr. Rasa Sabaliauskaitė1, prof. Sonata Jarmalaitė1
1 Nacionalinis vėžio institutas
2 Vilniaus universiteto Biomokslų instituto Gyvybės mokslų centras
Literatūra
1. Van Gorp T, et al. HE4 and CA125 as a diagnostic test in ovarian cancer: prospective validation of the Risk of Ovarian Malignancy Algorithm. Br J Cancer 2011. 104:863±70.https://doi.org/10.1038/sj.bjc.6606092 PMID: 21304524.
2. Bray F. et al. (2018). Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA: a cancer journal for clinicians, 68(6), p. 394–424. doi: 10.3322/caac.21492.
3. Andriole GL, et al. Prostate cancer screening in the randomized Prostate, Lung, Colorectal, and Ovarian Cancer Screening Trial: mortality results after 13 years of follow-up. J Natl Cancer Inst. 2012 Jan 18;104(2):125-32. doi: 10.1093/jnci/djr500. Epub 2012 Jan 6.
4. Thornton JG, Bewley S. Ovarian cancer screening: UKCTOCS trial.Lancet. 2016 Jun 25;387(10038):2601-2. doi: 10.1016/S0140-6736(16)30846-7.
5. Kurman RJ. (2013). Origin and molecular pathogenesis of ovarian high-grade serous carcinoma. 24(Supplement 10). doi: 10.1093/annonc/mdt463.
6. Kurman R J, Shih IM. (2012). Molecular Pathogenesis and Extraovarian Origin of Epithelial Ovarian Cancer. Shifting the Paradigm Access. 42(7), p. 918–931. doi: 10.1016/j.humpath.2011.03.003.Molecular.
7. Levine DA, Network TCGAR (2013). Integrated genomic characterization of endometrial carcinoma. Nature. Nature Publishing Group, 497(7447), p. 67–73. doi: 10.1038/nature12113.
8. Iijima M, et al. (2017). Genome-wide analysis of gynecologic cancer: The Cancer Genome Atlas in ovarian and endometrial cancer. Oncology letters. Spandidos Publications, 13(3), p. 1063–1070. doi: 10.3892/ol.2017.5582.
9. Soslow RA, et al. (2018). Endometrial Carcinoma Diagnosis: Use of FIGO Grading and Genomic Subcategories in Clinical Practice: Recommendations of the International Society of Gynecological Pathologists. 0, p. 64–74. doi: 10.1097/PGP.0000000000000518.
10. Kanopiene D, et al. (2015). Endometrial cancer and microsatellite instability status. Open medicine (Warsaw, Poland). De Gruyter Open, 10(1), p. 70–76. doi: 10.1515/med-2015-0005.
11. Schultheis, A. M. et al. (2016). TP53 Mutational Spectrum in Endometrioid and Serous Endometrial Cancers. International Journal of Gynecological Pathology, 35(4), p. 289–300. doi: 10.1097/PGP.0000000000000243.
12. Hafner A, et al. (2019). The multiple mechanisms that regulate p53 activity and cell fate. Nature Reviews Molecular Cell Biology. Springer US, 20(4), p. 199–210. doi: 10.1038/s41580-019-0110-x.
13. Brachova P, et al. (2015). TP53 oncomorphic mutations predict resistance to platinum- and taxane-based standard chemotherapy in patients diagnosed with advanced serous ovarian carcinoma. International Journal of Oncology, 46(2), p. 607–618. doi: 10.3892/ijo.2014.2747.
14. Bell D, et al. (2011). Integrated genomic analyses of ovarian carcinoma. Nature, 474(7353), p. 609–615. doi: 10.1038/nature10166.
15. Szajnik M, et al. (2016). Biological markers of prognosis, response to therapy and outcome in ovarian carcinoma. Expert review of molecular diagnostics. NIH Public Access, 16(8), p. 811–26. doi: 10.1080/14737159.2016.1194758.
16. Muinelo-Romay L, et al. (2018). Liquid biopsy in endometrial cancer: New opportunities for personalized oncology. International Journal of Molecular Sciences, 19(8). doi: 10.3390/ijms19082311.
17. Swisher EM, et al. (2005). Tumor-specific p53 sequences in blood and peritoneal fluid of women with epithelial ovarian cancer. American Journal of Obstetrics and Gynecology, 193(3), p. 662–667. doi: 10.1016/j.ajog.2005.01.054.
18. Erickson BK, et al. (2014). Detection of Somatic TP53 Mutations in Tampons of Patients With High-Grade Serous Ovarian Cancer. 124(5), p. 881–885. doi: 10.1097/AOG.0000000000000484.
19. Bakkum-gamez JN, et al. (2016). Detection of Endometrial Cancer via Molecular Analysis of DNA Collected with Vaginal Tampons Jamie. 137(November 2012), p. 14–22. doi: 10.1016/j.ygyno.2015.01.552.Detection.
20. Nair N, et al. (2016). Genomic Analysis of Uterine Lavage Fluid Detects Early Endometrial Cancers and Reveals a Prevalent Landscape of Driver Mutations in Women without Histopathologic Evidence of Cancer: A Prospective Cross-Sectional Study. PLoS Medicine, 13(12), p. 1–26. doi: 10.1371/journal.pmed.1002206.
21. Wang Y, et al. (2018). Evaluation of liquid from the Papanicolaou test and other liquid biopsies for the detection of endometrial and ovarian cancers. Science Translational Medicine, 10(433), p. eaap8793. doi: 10.1126/scitranslmed.aap8793.




